产品描述
HRbio™ qPCR SYBR Green Master Mix (No Rox) 是 2×实时定量 PCR 扩增的预混合溶液。Mix中含有热启动 HRbio™ DNA Polymerase、SYBR Green I、dNTPs、Mg2+。使用时仅需在扩增体系中加入模板和引物即可进行实时荧光定量 PCR,大大简化操作过程,降低污染几率。
本品采用的 DNA 聚合酶配体可以随温度变化实时调节 DNA 聚合酶活性。配方添加了有效抑制非特异性 PCR 扩增的因子和提升 PCR 反应扩增效率的因子,使定量 PCR 可以在宽广的定量区域内获得良好的线性关系。
适用机型
Bio-Rad: CFX96, CFX384, iCycler iQ, iQ5, MyiQ, MiniOpticon, Opticon, Opticon 2, Chromo4;
Eppendorf: Mastercycler ep realplex, realplex 2 s;
Qiagen: Corbett Rotor-Gene Q, Rotor-Gene 3000, Rotor-Gene 6000;
Roche Applied Science: LightCycler 480, LightCycler 2.0; Lightcycler 96;
Thermo Scientific: PikoReal Cycler; Cepheid: SmartCycler; Illumina: Eco qPCR.
运输和保存方法
冰袋运输。-20℃保存,有效期18个月。
本品避免反复冻融。产品中含有荧光染料 SYBR Green I,保存或配制反应体系时需避免强光照射。
注意事项
- 推荐使用本公司 cDNA 合成试剂盒,以有效去除 RNA样品中残留的基因组。
- 解冻后 Master Mix 可能出现絮状物质,4℃放置并上下颠倒混匀至溶液澄清,不影响试剂性能。
- 为了您的安全和健康,请穿实验服并佩戴一次性手套操作。
- 本产品仅作科研用途!
引物设计指南
1. 推荐引物长度25 bp 左右。扩增产物长度 150 bp 为佳,可以在 100 bp-300 bp 内选择。
2. 正向引物和反向引物的 Tm 值相差不宜超过 2℃。引物 Tm 值 60℃-65℃为佳。
3. 引物碱基分布要均匀,避免出现连续的 4 个相同碱基,GC 含量控制在 50%左右。3’端最后一个碱基最好为 G 或 C。
4. 引物内部或者正反两条引物间最好避免出现有 3 个碱基以上的互补序列。
5. 引物特异性需要用 NCBI BLAST 程序进行核对。避免引物 3’端有 2 个碱基以上的非特异性互补。
6. 设计完成的引物需要进行扩增效率的检测,只有具备相同扩增效率的引物才可用于定量比较分析。
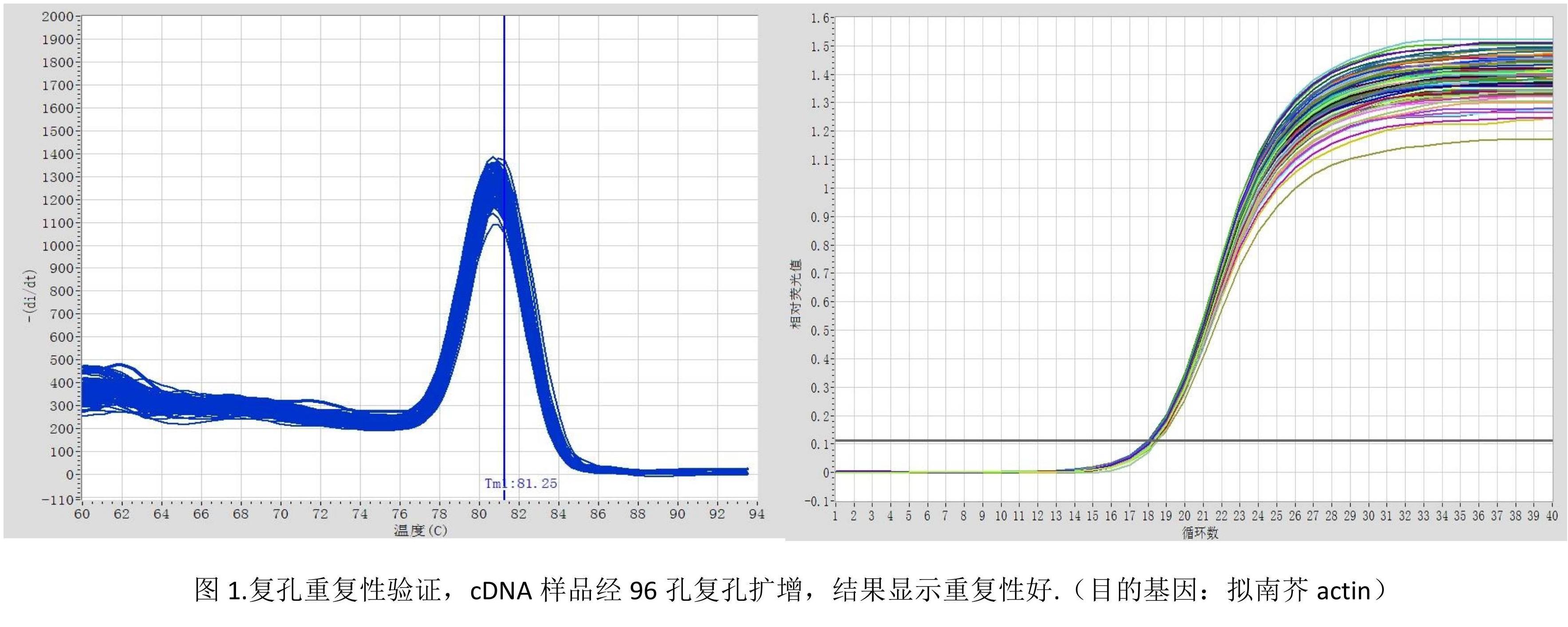
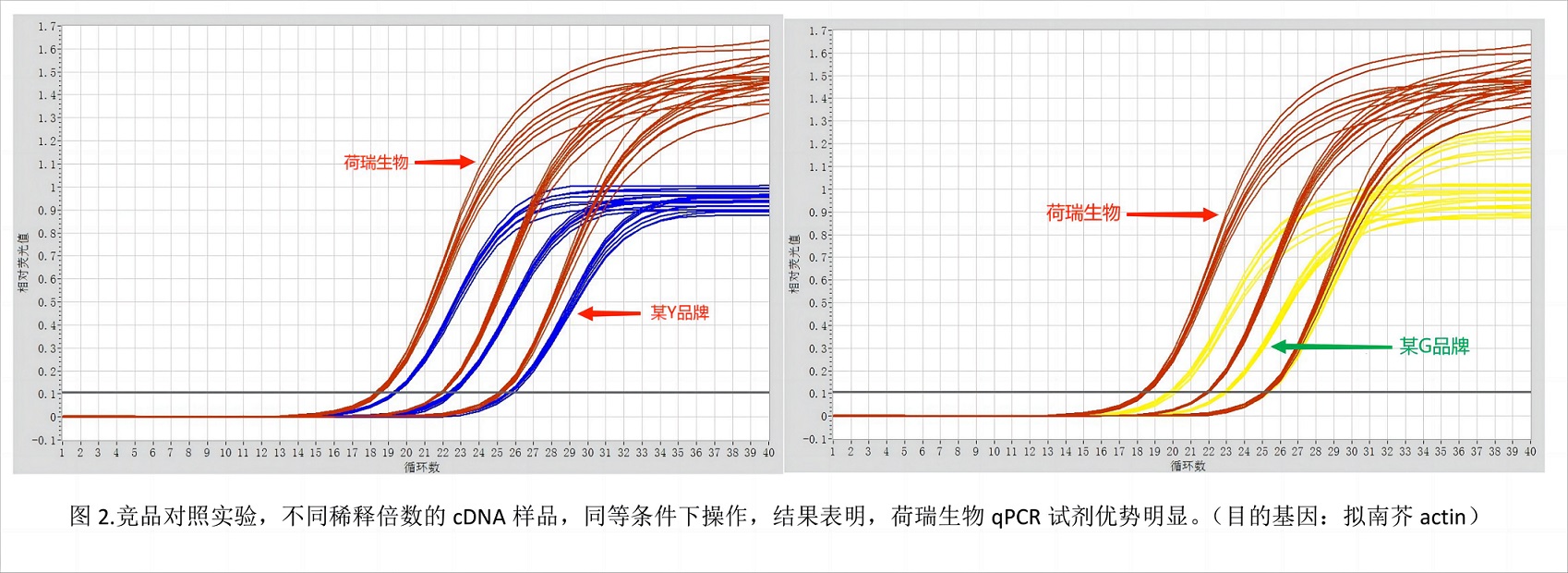
实验案例